تولید سولفات آمونیوم:

سولفات آمونیوم از تصفیه آمونیاک با اسید سولفوریک ساخته می شود:
2 NH3 + H2SO4 → (NH4) 2SO4
مخلوطی از گاز آمونیاک و بخار آب به یک راکتور وارد می شود، که حاوی محلول اشباع شده سولفات آمونیوم و حدود 2 تا 4٪ اسید سولفوریک آزاد در دمای 60 درجه سانتیگراد است. اسید سولفوریک غلیظ برای اسیدی نگه داشتن محلول و حفظ سطح اسید آزاد آن اضافه می شود.
گرمای واکنش دمای راکتور را در 60 درجه سانتیگراد نگه می دارد. سولفات آمونیوم خشک و پودر شده ممکن است با پاشش اسید سولفوریک در محفظه واکنش پر از گاز آمونیاک ایجاد شود. گرمای واکنش تمام آب موجود در سیستم را تبخیر می کند و یک نمک پودری تشکیل می دهد.
تقریباً 6000 میلیون تن در سال 1981 تولید شده است. سولفات آمونیوم از گچ نیز تولید می شود (CaSO4 · 2H2O). گچ ریز تقسیم شده به محلول کربنات آمونیوم اضافه می شود. کربنات کلسیم به صورت جامد رسوب می کند و سولفات آمونیوم را در محلول می گذارد.
(NH4) 2CO3 + CaSO4 → (NH4) 2SO4 + CaCO3
سولفات آمونیوم به طور طبیعی به عنوان ماده ماساژیت معدنی کمیاب در بخارات آتشفشانی و به دلیل آتش سوزی ذغال سنگ در برخی از زباله ها تولید می شود.
ساختار سولفات آمونیوم:
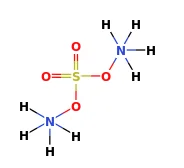
ماهیت شیمیایی سولفات آمونیوم:
شاید این سوال برای شما نیز به وجود آمده که آیا سولفات آمونیوم اسید است یا باز؟
واکنش بین اسید سولفوریک و هیدروکسید آمونیوم باعث تولید سولفات آمونیوم می شود. اسید سولفوریک یک اسید قوی و هیدروکسید آمونیوم یک پایه ضعیف است. بنابراین نمک تشکیل شده توسط سولفات آمونیوم اسیدی است.














