شیمی عمومی باتری:
یک باتری دارای سه لایه ی کاتد، آند و جداکننده است. لایه منفی باتری، آند و لایه مثبت آن، کاتد نامیده می شود.

هنگامی که یک بار الکتریکی به باتری اضافه شود، جریان از آند به کاتد شارش می یابد. به طور مشابه، هنگامی که شارژر باتری را وصل کنیم، جریان در جهت مخالف یعنی از کاتد به آند شروع به شارش می کند.
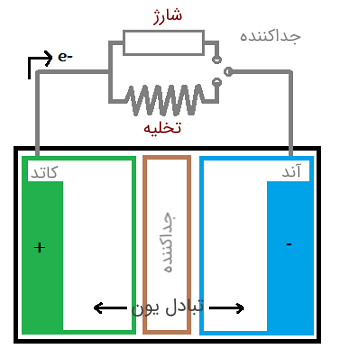
هر باتری بر اساس یک واکنش شیمیایی، یعنی واکنش اکسایش-کاهش کار می کند. این واکنش بین کاتد و آند و از طریق جداکننده (الکترولیت) رخ می دهد.
در نتیجه، یک الکترود به علت واکنش اکسایش به صورت منفی باردار می شود. این الکترود، کاتد نام دارد. الکترود دیگر به علت واکنش کاهش به صورت مثبت باردار می شود که آن را آند می نامند.
هنگامی که دو نوع فلز مختلف در محلول الکترولیت یکسانی فرو برده شوند، یکی از الکترودها الکترون می گیرد و دیگری الکترون از دست می دهد.
در نتیجه، یکی از فلزها الکترون می گیرد و دیگری الکترون از دست خواهد داد. این اختلاف در تراکم الکترون دو فلز، بین فلزها اختلاف پتانسیل الکتریکی ایجاد می کند.
این اختلاف پتانسیل می تواند به عنوان منبع ولتاژ در هر وسیله الکتریکی استفاده شود. یون ها فقط از طریق جداکننده جریان می یابند و جداکننده تمام حرکات از آند به کاتد را مسدود می کند. بنابراین، تنها راه دریافت جریان خارجی، از طریق پایانه های باتری است.
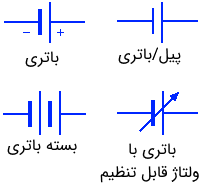
شکل زیر چند نماد مربوط به باتری ها را نشان می دهد.